अध्याय 08 रेडॉक्स प्रतिक्रियाएँ
“जहाँ ऑक्सीकरण होता है, वहाँ हमेशा कमी होती है। रसायन विज्ञान मूल रूप से रेडॉक्स प्रणालियों का अध्ययन करता है।”
रसायन विज्ञान सामग्री के विभिन्न प्रकार और एक प्रकार की सामग्री के दूसरे प्रकार में परिवर्तन के बारे में है। सामग्री का एक प्रकार से दूसरे प्रकार में परिवर्तन विभिन्न प्रकार की प्रतिक्रियाओं के माध्यम से होता है। ऐसी प्रतिक्रियाओं के एक महत्वपूर्ण श्रेणी के रूप में रेडॉक्स प्रतिक्रियाएँ हैं। रेडॉक्स प्रतिक्रियाओं से संबंधित भौतिक और जैविक दोनों प्रकार के अनेक घटनाएँ हैं। ये प्रतिक्रियाएँ फार्मास्युटिकल, जैविक, औद्योगिक, वर्णशास्त्रीय और कृषि क्षेत्रों में व्यापक रूप से उपयोग की जाती हैं। इन प्रतिक्रियाओं का महत्व इस बात से स्पष्ट है कि घरेलू, परिवहन और अन्य वाणिज्यिक उद्देश्यों के लिए ऊर्जा प्राप्त करने के लिए विभिन्न प्रकार के ईंधन की ज्वार, उच्च प्रतिक्रियाशील धातुओं और अधातुओं के निकालन के लिए इलेक्ट्रोकेमिकल प्रक्रियाओं, कौस्टिक सोडा जैसे रासायनिक यौगिकों का निर्माण, सूखी और आर्द्र बैटरीयों के संचालन और धातुओं की विघटन इन रेडॉक्स प्रक्रियाओं के अंतर्गत आती हैं। हाल के समय में, पर्यावरणीय मुद्दे जैसे हाइड्रोजन अर्थव्यवस्था (ईंधन के रूप में द्रव हाइड्रोजन का उपयोग) और ‘ओजोन छेद’ का विकास रेडॉक्स घटना के तहत शामिल होने लगे हैं।
8.1 रेडॉक्स प्रतिक्रियाओं की पारंपरिक विचारधारा - ऑक्सीकरण और कमी प्रतिक्रियाएँ
मूल रूप से, ऑक्सीकरण शब्द का उपयोग एक तत्व या यौगिक में ऑक्सीजन के जोड़ने का वर्णन करने के लिए किया जाता था। आस्मोस्फ़ीर में डाइऑक्सीजन (20%) के उपस्थिति के कारण, अनेक तत्व इससे जुड़ जाते हैं और यही कारण है कि ये तत्व आमतौर पर पृथ्वी पर अपने ऑक्साइड के रूप में पाए जाते हैं। निम्नलिखित प्रतिक्रियाएँ ऑक्सीकरण प्रक्रियाओं का प्रतिनिधित्व करती हैं अंतर्निहित ऑक्सीकरण की परिभाषा के अनुसार:
$$2 \mathrm{Mg}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{MgO}(\mathrm{s}) \tag{8.1}$$
$$\mathrm{S}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow \mathrm{SO_2}(\mathrm{~g}) \tag{8.2}$$
प्रतिक्रियाओं (8.1) और (8.2) में, मैग्नीशियम और सल्फर तत्वों में ऑक्सीजन के जोड़ने के कारण ऑक्सीकरण होता है। इसी प्रकार, मेथन के ऑक्सीकरण का कारण उसमें ऑक्सीजन के जोड़ने है।
$$\mathrm{CH} _{4}(\mathrm{~g})+2 \mathrm{O} _{2}(\mathrm{~g}) \rightarrow \mathrm{CO} _{2}(\mathrm{~g})+2 \mathrm{H} _{2} \mathrm{O}(\mathrm{l}) \tag{7.3}$$
प्रतिक्रिया (8.3) में जहाँ हाइड्रोजन को ऑक्सीजन द्वारा बदल दिया गया है, इसकी सावधानी से जांच ने रसायनशास्त्रीों को हाइड्रोजन को इससे हटाने के रूप में ऑक्सीकरण की पुनर्व्याख्या करने के लिए प्रेरित किया और इस प्रकार, ऑक्सीकरण शब्द का अर्थ एक यौगिक से हाइड्रोजन को हटाने को शामिल करने के लिए विस्तारित किया गया। निम्नलिखित उदाहरण एक अन्य प्रतिक्रिया है जहाँ हाइड्रोजन को हटाने को भी ऑक्सीकरण प्रतिक्रिया के रूप में उल्लेख किया जा सकता है।
$$ \begin{equation*} 2 \mathrm{H_2} \mathrm{~S}(\mathrm{~g})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{~S}(\mathrm{~s})+2 \mathrm{H_2} \mathrm{O}(\mathrm{l}) \tag{8.4} \end{equation*} $$
रसायनशास्त्रीों की ज्ञान की वृद्धि के कारण, ऑक्सीकरण शब्द को उन प्रतिक्रियाओं के लिए विस्तारित किया गया जो (7.1 से 7.4) ऑक्सीजन के बिना अन्य नाइट्रोजनीय तत्वों के उपयोग के साथ होती हैं। मैग्नीशियम का फ्लोरीन, क्लोरीन और सल्फर जैसे तत्वों के साथ ऑक्सीकरण निम्नलिखित प्रतिक्रियाओं के अनुसार होता है:
$$\operatorname{Mg}(\mathrm{s})+\mathrm{F_2} (\mathrm{~g}) \rightarrow \operatorname{MgF_2} (s) \tag{8.5}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{Cl_2} (g) \rightarrow \mathrm{MgCl_2} (s) \tag{8.6}$$
$$\mathrm{Mg}(\mathrm{s})+\mathrm{S} (s) \rightarrow \operatorname{MgS}(\mathrm{s}) \tag{8.7}$$
प्रतिक्रियाओं (7.5 से 7.7) को ऑक्सीकरण प्रतिक्रियाओं के अंतर्गत शामिल करने ने रसायनशास्त्रीों को अपने आप में यह सोचने के लिए प्रेरित किया कि ऑक्सीकरण के रूप में हाइड्रोजन को हटाने के अलावा, इलेक्ट्रोपॉजिटिव तत्वों को हटाने को भी ऑक्सीकरण माना जा सकता है। इस प्रकार, निम्नलिखित प्रतिक्रिया:
$$ 2 \mathrm{~K_4} \left[ \mathrm{Fe} ( \mathrm{CN})_{6} \right] ( \mathrm{aq}) + \mathrm{H_2} \mathrm{O_2} ( \mathrm{aq}) \rightarrow 2 \mathrm{~K_3} \left[\mathrm{Fe}( \mathrm{CN})_6 \right] ( \mathrm{aq}) + 2 \mathrm{KOH} ( \mathrm{aq}) $$
के अनुसार पोटाशियम फेरोसाइनेट से पोटाशियम फेर्रोसाइनेट में परिवर्तन होने से पहले इलेक्ट्रोपॉजिटिव तत्व पोटाशियम को हटाने के कारण ऑक्सीकरण के रूप में व्याख्या की जाती है। सारांश में, “ऑक्सीकरण” शब्द को यौगिक में ऑक्सीजन/नाइट्रोजनीय तत्व के जोड़ने या हाइड्रोजन/इलेक्ट्रोपॉजिटिव तत्व को हटाने के रूप में परिभाषित किया जाता है।
शुरुआत में, कमी को एक यौगिक से ऑक्सीजन को हटाने के रूप में माना जाता था। हालाँकि, कमी शब्द का अर्थ आज के दिन विस्तारित किया गया है जिसमें यौगिक से ऑक्सीजन/नाइट्रोजनीय तत्व को हटाने या हाइड्रोजन/इलेक्ट्रोपॉजिटिव तत्व को जोड़ने को शामिल किया गया है।
उपरोक्त परिभाषा के अनुसार, निम्नलिखित कमी प्रक्रियाओं के उदाहरण हैं:
$$2 \mathrm{HgO}(\mathrm{s}) \xrightarrow{\Delta} 2 \mathrm{Hg}(\mathrm{l})+\mathrm{O_2}(\mathrm{~g}) \tag{8.8}$$
(मेरकुरिक ऑक्साइड से ऑक्सीजन को हटाना)
$$2 \mathrm{FeCl_3}(\mathrm{aq})+\mathrm{H_2}(\mathrm{~g}) \rightarrow 2 \mathrm{FeCl_2}(\mathrm{aq})+2 \mathrm{HCl}(\mathrm{aq}) \tag{8.9}$$
(फेरिक क्लोराइड से नाइट्रोजनीय तत्व, क्लोरीन को हटाना)
$$\mathrm{CH_2}=\mathrm{CH_2}(\mathrm{~g})+\mathrm{H_2}(\mathrm{~g}) \rightarrow \mathrm{H_3} \mathrm{C}-\mathrm{CH_3}(\mathrm{~g})\tag{8.10}$$
(हाइड्रोजन के जोड़ना)
$$2 \mathrm{HgCl_2}(\mathrm{aq})+\mathrm{SnCl_2}(\mathrm{aq}) \rightarrow \mathrm{Hg_2} \mathrm{Cl_2}(\mathrm{~s})+\mathrm{SnCl_4}(\mathrm{aq})\tag{8.11}$$
(मेरकुरिक क्लोराइड में मेरकुरी के जोड़ना)
प्रतिक्रिया (8.11) में, स्टैनोस क्लोराइड के स्टैनिक क्लोराइड में परिवर्तन के कारण इसमें नाइट्रोजनीय तत्व क्लोरीन के जोड़ने के कारण सहसंबंध ऑक्सीकरण भी होता है। जल्दी से पता चला कि ऑक्सीकरण और कमी हमेशा सहसंबंध में होती हैं (जैसा कि ऊपर दिए गए सभी समीकरणों को फिर से जांचकर स्पष्ट होगा), इसलिए इस प्रकार की रासायनिक प्रतिक्रियाओं के लिए “रेडॉक्स” शब्द बनाया गया।
समस्या 8.1
निम्नलिखित प्रतिक्रियाओं में, ऑक्सीकरण और कमी में परिवर्तन करने वाली पदार्थ की पहचान करें:
(i) $\mathrm{H_2} \mathrm{~S}$ (g) $+\mathrm{Cl_2}$ (g) $\rightarrow 2 \mathrm{HCl}$ (g) $+\mathrm{S}$ (s)
(ii) $3 \mathrm{Fe_3} \mathrm{O_4}$ (s) $+8 \mathrm{Al}$ (s) $\rightarrow 9 \mathrm{Fe}$ (s) $+4 \mathrm{Al_2} \mathrm{O_3}(\mathrm{~s})$
(iii) $2 \mathrm{Na}$ (s) $+\mathrm{H_2}$ (g) $\rightarrow 2 \mathrm{NaH}$ (s)
समाधान
(i) $\mathrm{H_2} \mathrm{~S}$ ऑक्सीकरण होता है क्योंकि एक अधिक नाइट्रोजनीय तत्व, क्लोरीन हाइड्रोजन में जुड़ जाता है (या एक अधिक इलेक्ट्रोपॉजिटिव तत्व, हाइड्रोजन से स को हटा दिया गया है)। क्लोरीन कमी में परिवर्तित होता है क्योंकि इसमें हाइड्रोजन के जोड़ने के कारण।
(ii) अल्युमीनियम ऑक्सीकरण होता है क्योंकि इसमें ऑक्सीजन के जोड़ने के कारण। फेरोफेरिक ऑक्साइड $\left(\mathrm{Fe_3} \mathrm{O_4}\right)$ कमी में परिवर्तित होता है क्योंकि इससे ऑक्सीजन को हटा दिया गया है।
(iii) नाइट्रोजनीयता के संकेत के ध्यान से अनुप्रयोग करके ही हम यह निष्कर्ष निकाल सकते हैं कि सोडियम ऑक्सीकरण होता है और हाइड्रोजन कमी में परिवर्तित होता है।
यहाँ चुनी गई प्रतिक्रिया (iii) हमें रेडॉक्स प्रतिक्रियाओं को परिभाषित करने के एक अन्य तरीके पर सोचने के लिए प्रेरित करती है।
8.2 इलेक्ट्रॉन हस्तांतरण प्रतिक्रियाओं के रूप में रेडॉक्स प्रतिक्रियाएँ
हम पहले ही सीख चुके हैं कि प्रतिक्रियाएँ रेडॉक्स प्रतिक्रियाएँ हैं क्योंकि इनमें सभी प्रतिक्रियाओं में सोडियम ऑक्सीकरण होता है चाहे यह सोडियम में ऑक्सीजन या अधिक नाइट्रोजनीय तत्व के जोड़ने के कारण हो।
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{NaCl}(\mathrm{s})\tag{8.12}$$
$$4 \mathrm{Na}(\mathrm{s})+\mathrm{O_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na_2} \mathrm{O}(\mathrm{s})\tag{8.13}$$
$$2 \mathrm{Na}(\mathrm{s})+\mathrm{S}(\mathrm{s}) \rightarrow \mathrm{Na_2} \mathrm{~S}(\mathrm{~s}) \tag{8.14}$$
इसी समय, क्लोरीन, ऑक्सीजन और सल्फर कमी में परिवर्तित होते हैं क्योंकि इनमें सभी में इलेक्ट्रोपॉजिटिव तत्व सोडियम के जोड़ने के कारण। हमारे रासायनिक बंधन के बारे में ज्ञान के साथ-साथ हमें यह भी पता है कि सोडियम क्लोराइड, सोडियम ऑक्साइड और सोडियम सल्फाइड आयनिक यौगिक हैं और शायद बेहतर रूप से $\mathrm{Na}^{+} \mathrm{Cl}^{-}( \mathrm{s}),\left(\mathrm{Na}^{+} \right)_2 \mathrm{O}^{2-}( \mathrm{s})$, $ \left(\mathrm{Na}^{+} \right)_2$ $\mathrm{S}^{2-}( \mathrm{s})$ के रूप में लिखा जा सकता है। उत्पन्न पदार्थों पर आवेश का विकास हमें प्रतिक्रियाओं (8.12 से 8.14) को निम्नलिखित तरीके से फिर से लिखने के लिए प्रेरित करता है:
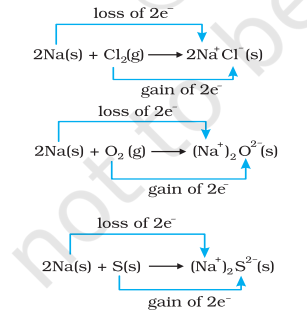
आसानी के लिए, उपरोक्त प्रक्रियाओं में से प्रति प्रक्रिया को दो अलग-अलग चरणों में विभाजित माना जा सकता है, एक जिसमें इलेक्ट्रॉनों का हार होता है और दूसरा जिसमें इलेक्ट्रॉनों का लाभ होता है। एक उदाहरण के लिए, हम इनमें से एक को और विस्तृत कर सकते हैं, जैसे कि सोडियम क्लोराइड का निर्माण।
$2 \mathrm{Na}(\mathrm{s}) \rightarrow 2 \mathrm{Na}^{+}(\mathrm{g})+2 \mathrm{e}^{-}$
$\mathrm{Cl_2}(\mathrm{~g})+2 \mathrm{e}^{-} \rightarrow 2 \mathrm{Cl}^{-}(\mathrm{g})$
उपरोक्त प्रत्येक चरण को अर्ध प्रतिक्रिया कहा जाता है, जो इलेक्ट्रॉनों के भागीदारी को स्पष्ट रूप से दिखाता है। अर्ध प्रतिक्रियाओं का योग कुल प्रतिक्रिया देता है:
$2 \mathrm{Na}(\mathrm{s})+\mathrm{Cl_2}(\mathrm{~g}) \rightarrow 2 \mathrm{Na}^{+} \mathrm{Cl}^{-}(\mathrm{s})$ या $2 \mathrm{NaCl}(\mathrm{s})$
प्रतिक्रियाएँ 8.12 से 8.14 सुझाव देती हैं कि इलेक्ट्रॉनों के हारने वाली अर्ध प्रतिक्रियाएँ ऑक्सीकरण प्रतिक्रियाएँ कहलाती हैं। इसी प्रकार, इलेक्ट्रॉनों के लाभार्जित करने वाली अर्ध प्रतिक्रियाएँ कमी प्रतिक्रियाएँ कहलाती हैं। यह भी उपवज्जा में उल्लेख करना सही नहीं होगा कि ऑक्सीकरण और कमी की नई परिभाषा केवल पदार्थों के व्यवहार के आधार पर पारंपरिक विचारधारा और इलेक्ट्रॉन-हस्तांतरण परिवर्तन के बीच संबंध की स्थापना करके ही हासिल की गई है। प्रतिक्रियाएँ (8.12 से 8.14) में सोडियम, जो ऑक्सीकरण होता है, एक कमजोरी के उपकरण के रूप में कार्य करता है क्योंकि यह अपने साथ में इलेक्ट्रॉन देकर उन तत्वों को कम करने में मदद करता है जिनके साथ इसका संपर्क होता है। क्लोरीन, ऑक्सीजन और सल्फर कमी में परिवर्तित होते हैं और ऑक्सीकरण के उपकरण के रूप में कार्य करते हैं क्योंकि ये सोडियम से इलेक्ट्रॉन लेते हैं। सारांश में, हम उल्लेख कर सकते हैं कि
ऑक्सीकरण: किसी भी पदार्थ द्वारा इलेक्ट्रॉन(ों) का हार।
कमी: किसी भी पदार्थ द्वा�








